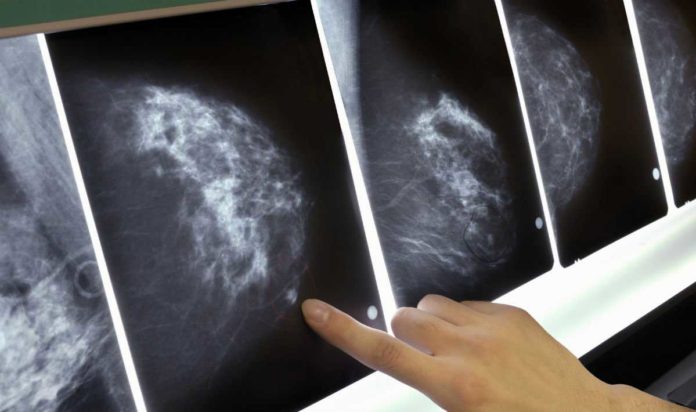
Di una grave e apparentemente incurabile forma di cancro metastatico al seno si può guarire e tornare alla vita normale senza nemmeno sottoporsi a cure invasive e debilitanti grazie all’immunoterapia. L’innovativo approccio immunologico sviluppato dai ricercatori medici del National Institute of Health (Nci) di Bethesda, in Maryland su una donna di 52 anni è stato un successo e i risultati della ricerca sono stati pubblicati sulla rivista Nature Medicine e dalla Società Americana di Oncologia Clinica (Asco).
Il caso risale al 2013, quando la donna aveva avuta diagnosticata una speranza di vita di appena tre mesi, visto che il suo cancro al seno, nonostante l’asportazione, aveva generato metastasi diffondendosi i tutto il corpo. A nulla sono valsi i cicli di chemioterapia, ma la tempra della paziente, alla fine, ha avuto la meglio grazie alla cura applicata per la prima volta che prevede un trattamento di immunoterapia rivoluzionario, il cosiddetto “trasferimento cellulare adottivo”. Un trattamento capace di dare nuova linfa vitale alla paziente, pesantemente compromessa dalla chemioterapia, tanto che nel giro di un paio di settimane di trattamento si sono registrati i primi miglioramenti, tra la felicità della paziente e dei medici curanti. Anche i risultati clinici basati su indagini chimiche, istologiche e radiologiche dimostravano il progressivo successo della cura.
Ora, a 22 mesi dalla fine del trattamento di immunoterapia, tempo ritenuto dai medici il minimo per valutare la portata delle cure, la paziente è completamente ristabilita e non ci sono tracce di cancro nel suo organismo.
Il risultato rivoluzionario della cura è stato possibile cambiando approccio e coinvolgendo la genetica medica. Le cellule di difesa immunitaria della paziente malata, i globuli bianchi, sono stati prelevati dal sangue, isolati, modificati geneticamente, riattivati, moltiplicati in vitro e reiniettati nelle sue vene con una flebo. I globuli bianchi, opportunamente potenziati e moltiplicati nel numero di ben 82 miliardi di linfociti “T”, hanno avuto la meglio sul tumore che aveva avuto nel tempo ben 62 mutazioni. Istruendo a dovere il sistema immunitario della paziente tramite i globuli bianchi modificati, questo è stato in grado di combattere tutte le cellule maligne, comprese le metastasi, nel giro di poche settimane.
La cura applicata alla paziente deriva da una forma modificata della “terapia cellulare adottiva”, già rivelatasi efficace nel trattamento del melanoma maligno, ma finora era considerata poco potente contro i tumori cosiddetti “freddi”, ovvero quelli resistenti alle comuni terapie dello stomaco, dell’esofago, delle ovaie e, appunto, del seno. I linfociti infiltranti il tumore, chiamati “Til”, sono stati cioè coltivati in grande quantità in laboratorio, modificati con l’ingegneria genetica in modo da diventare capaci di bersagliare specificatamente le mutazioni delle cellule tumorali, e poi reinfusi nell’organismo mediante una semplice trasfusione, creando in tal modo una formidabile risposta immunitaria contro il tumore da distruggere.
Se i dati saranno confermati nei prossimi mesi, arricchiti con studi più ampi, questo approccio terapeutico sarà esteso ulteriormente ad un più ampio spettro di tumori resistenti alle terapie classiche, quelli cioè considerati senza speranze.
Anche se il trattamento di immunoterapia è stato sperimentato su un solo caso considerato terminale, si è comunque accertato in modo incontrovertibile che l’azione terapeutica è stata vincente, aprendo così nuove ed importanti prospettive per la cura dei tumori in stadio avanzato e in presenza di metastasi, dando una speranza di vita a migliaia di pazienti nel mondo considerati senza speranza.